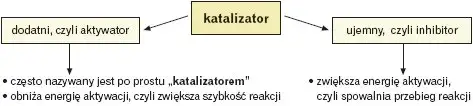
Katalizator to substancja, która przyspiesza reakcje chemiczne, nie ulegając przy tym trwałym zmianom. Działa poprzez obniżenie energii aktywacji, czyli minimalnej energii potrzebnej do rozpoczęcia reakcji. Dzięki temu procesy chemiczne zachodzą szybciej i efektywniej, co ma ogromne znaczenie zarówno w laboratoriach, jak i w przemyśle.
W tym artykule wyjaśnimy, czym dokładnie jest katalizator, jak wpływa na przebieg reakcji oraz gdzie znajduje zastosowanie. Przedstawimy również przykłady katalizatorów, które spotykamy na co dzień, oraz omówimy ich rolę w nowoczesnej chemii. Jeśli chcesz zrozumieć, dlaczego katalizatory są tak ważne, czytaj dalej!
Kluczowe informacje:- Katalizator przyspiesza reakcje chemiczne, nie zużywając się w trakcie procesu.
- Obniża energię aktywacji, co sprawia, że reakcje zachodzą szybciej i przy niższych kosztach energetycznych.
- Stosowany jest zarówno w laboratoriach, jak i w przemyśle, np. w produkcji tworzyw sztucznych czy paliw.
- Przykłady katalizatorów to enzymy w organizmach żywych czy metale szlachetne w przemyśle chemicznym.
- Katalizatory mają kluczowe znaczenie dla rozwoju zrównoważonych technologii i ochrony środowiska.
Czym jest katalizator i jak działa w reakcjach chemicznych?
Katalizator to substancja, która przyspiesza reakcje chemiczne, nie ulegając przy tym trwałym zmianom. Działa poprzez obniżenie energii aktywacji, czyli minimalnej energii potrzebnej do rozpoczęcia reakcji. Dzięki temu procesy chemiczne zachodzą szybciej i efektywniej, co ma ogromne znaczenie zarówno w laboratoriach, jak i w przemyśle.
| Nazwa katalizatora | Typ reakcji | Prędkość przyspieszenia (x) | Zastosowanie |
|---|---|---|---|
| Platyna | Utlenianie | 1000x | Przemysł petrochemiczny |
| Enzymy | Hydroliza | 10 000x | Procesy biologiczne |
| Nikiel | Uwodornienie | 500x | Produkcja margaryny |
| Katalizator Vanadylowy | Utlenianie SO2 | 200x | Produkcja kwasu siarkowego |
| Zeolity | Krakowanie | 300x | Przetwórstwo ropy naftowej |
Rola katalizatora w przyspieszaniu reakcji chemicznych
Katalizator działa jak "pomocnik" w reakcjach chemicznych. Obniża energię aktywacji, co sprawia, że cząsteczki łatwiej przechodzą w stan przejściowy. Dzięki temu reakcje zachodzą szybciej, nawet w niższych temperaturach.
W przemyśle rola katalizatora jest nie do przecenienia. Pozwala na oszczędność energii, redukuje koszty produkcji i zwiększa wydajność procesów. Przykładowo, w produkcji amoniaku katalizator żelazowy skraca czas reakcji z kilku godzin do kilku minut.
Przykłady katalizatorów w codziennym życiu i przemyśle
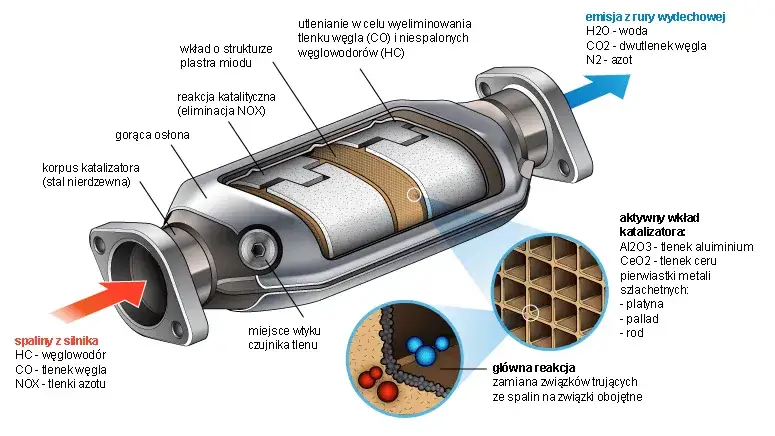
Katalizatory są obecne w wielu dziedzinach życia. W samochodach katalizatory platynowe oczyszczają spaliny, a w organizmach żywych enzymy przyspieszają trawienie. W przemyśle chemicznym katalizatory są kluczowe do produkcji tworzyw sztucznych, leków i paliw.
- Platyna – stosowana w katalizatorach samochodowych do redukcji szkodliwych gazów.
- Enzymy – przyspieszają reakcje metaboliczne w organizmach żywych.
- Nikiel – używany w procesie uwodornienia tłuszczów do produkcji margaryny.
- Zeolity – stosowane w przemyśle petrochemicznym do krakowania ropy naftowej.
Jak katalizator wpływa na energię aktywacji reakcji?
Energia aktywacji to kluczowy parametr w reakcjach chemicznych. Katalizator obniża tę wartość, tworząc alternatywną ścieżkę reakcji. Dzięki temu cząsteczki potrzebują mniej energii, aby przejść w stan przejściowy.
W praktyce oznacza to, że reakcje zachodzą szybciej i przy niższych temperaturach. Na przykład, bez katalizatora produkcja amoniaku wymagałaby temperatury 500°C, a z katalizatorem wystarczy 400°C. To ogromna oszczędność energii!
Czytaj więcej: Co to jest chemia i dlaczego warto ją zrozumieć w życiu codziennym
Dlaczego katalizatory są niezbędne w nowoczesnej chemii?
Katalizatory są fundamentem nowoczesnej chemii. Bez nich wiele procesów przemysłowych byłoby niemożliwych lub zbyt kosztownych. W produkcji leków katalizatory pozwalają na precyzyjne kontrolowanie reakcji, co przekłada się na wyższą jakość produktów.
W przemyśle petrochemicznym katalizatory są kluczowe do przekształcania ropy naftowej w paliwa i tworzywa sztuczne. Dzięki nim możliwe jest również tworzenie nowych materiałów, takich jak biodegradowalne polimery, które są przyjazne dla środowiska.
Pamiętaj, że wybór odpowiedniego katalizatora zależy od rodzaju reakcji. Niektóre katalizatory działają tylko w określonych warunkach, np. w wysokich temperaturach lub w obecności określonych substancji.
Czy katalizatory mogą ulec zużyciu? Wady i ograniczenia
Choć katalizatory nie zużywają się w trakcie reakcji, mogą tracić skuteczność. Proces ten nazywany jest "dezaktywacją". Przyczyną może być zanieczyszczenie powierzchni katalizatora lub zmiana jego struktury w wyniku wysokich temperatur.
W przemyśle problemem jest również koszt katalizatorów. Niektóre, jak platyna, są bardzo drogie. Dodatkowo, ich regeneracja często wymaga skomplikowanych procesów, co zwiększa koszty produkcji. Mimo to korzyści przewyższają te ograniczenia.
Jak wybrać odpowiedni katalizator do konkretnej reakcji?
 Wybór katalizatora zależy od rodzaju reakcji i warunków, w jakich ma zachodzić. Kluczowe jest dopasowanie właściwości katalizatora do potrzeb procesu. Na przykład, w reakcjach utleniania często stosuje się metale szlachetne, takie jak platyna czy pallad.
Wybór katalizatora zależy od rodzaju reakcji i warunków, w jakich ma zachodzić. Kluczowe jest dopasowanie właściwości katalizatora do potrzeb procesu. Na przykład, w reakcjach utleniania często stosuje się metale szlachetne, takie jak platyna czy pallad.
Przed wyborem katalizatora warto przeprowadzić testy laboratoryjne. Sprawdź, jak reaguje on w różnych warunkach temperaturowych i ciśnieniowych. To pozwoli uniknąć niepotrzebnych kosztów i problemów w przyszłości.
Przyszłość katalizatorów: innowacje i nowe technologie
Nowoczesne katalizatory są coraz bardziej wydajne i przyjazne dla środowiska. Naukowcy pracują nad materiałami, które działają w niższych temperaturach i są łatwiejsze w regeneracji. Przykładem są katalizatory oparte na nanotechnologii.
W przyszłości katalizatory mogą zrewolucjonizować produkcję energii. Badane są już katalizatory do efektywnego rozkładu wody na wodór i tlen, co mogłoby zapewnić czyste źródło energii. To tylko jeden z wielu obiecujących kierunków rozwoju.
Najczęstsze błędy w rozumieniu działania katalizatorów
Wiele osób myśli, że katalizatory zużywają się w trakcie reakcji. To nieprawda – pozostają niezmienione chemicznie. Innym błędem jest przekonanie, że każdy katalizator działa w każdych warunkach. W rzeczywistości są one bardzo specyficzne.
- Katalizator nie zmienia równowagi reakcji, tylko przyspiesza jej osiągnięcie.
- Nie wszystkie katalizatory działają w niskich temperaturach – niektóre wymagają wysokich wartości.
- Katalizatory nie są uniwersalne – każdy typ ma swoje specyficzne zastosowania.
Jak katalizatory wpływają na środowisko naturalne?
Katalizatory mają ogromny wpływ na ochronę środowiska. W samochodach redukują emisję szkodliwych gazów, a w przemyśle chemicznym pozwalają na bardziej ekologiczne procesy. Dzięki nim możliwe jest również wytwarzanie biodegradowalnych materiałów.
Jednak niektóre katalizatory, zwłaszcza te zawierające metale ciężkie, mogą stanowić zagrożenie dla środowiska. Dlatego ważne jest odpowiednie zarządzanie odpadami i recykling zużytych katalizatorów.
Podsumowanie: kluczowe fakty o katalizatorach w chemii
Katalizatory to niezwykle ważne narzędzia w chemii. Przyspieszają reakcje, obniżają koszty produkcji i przyczyniają się do ochrony środowiska. Ich rola w przemyśle i badaniach naukowych jest niezastąpiona.
Od enzymów w organizmach żywych po metale szlachetne w przemyśle – katalizatory są wszędzie. Dzięki nim możliwe są innowacje, takie jak czystsze paliwa czy nowe materiały. To właśnie one napędzają postęp w nowoczesnej chemii.
Katalizatory: klucz do efektywności i ekologii w chemii
Katalizatory odgrywają kluczową rolę w przyspieszaniu reakcji chemicznych, obniżaniu kosztów produkcji i ochronie środowiska. Jak pokazano w artykule, ich działanie polega na obniżeniu energii aktywacji, co pozwala na szybsze i bardziej efektywne procesy. Przykłady, takie jak platyna w katalizatorach samochodowych czy enzymy w organizmach żywych, ilustrują ich wszechstronne zastosowanie.
Mimo że katalizatory nie zużywają się w trakcie reakcji, mogą tracić skuteczność przez zanieczyszczenia lub wysokie temperatury. Jednak ich korzyści, takie jak redukcja emisji szkodliwych gazów czy możliwość produkcji biodegradowalnych materiałów, przewyższają te ograniczenia. Nowoczesne technologie, takie jak katalizatory oparte na nanotechnologii, otwierają nowe możliwości dla przemysłu i ochrony środowiska.
Podsumowując, katalizatory są niezbędne zarówno w laboratoriach, jak i w przemyśle. Ich rola w rozwoju zrównoważonych technologii i efektywnych procesów chemicznych jest niezastąpiona, co czyni je fundamentem nowoczesnej chemii.